像玩乐高一样造原子:揭秘微观世界的“建筑学”
很多学生在初学化学时,都会被“质子、中子、电子”这些名词搞得头晕脑胀。课本上的平面图总是显得枯燥无味,难以想象这些微粒是如何构成我们眼前的万物。
他们会问:
- 为什么有的原子带电,有的不带电?
- 为什么改变一个电子,元素没有变;但改变一个质子,元素就变了?
- “同位素”到底是什么?
- 原子为什么会稳定?
这些问题,单靠课本里的二维图,很难解释清楚。
所以我在上课时,经常会使用科罗拉多大学开发的 PhET 互动模拟器: “Build an Atom”。
学生不是“看”原子,而是真正自己把一个原子搭出来。
学生在模拟里到底做什么?

这个模拟非常简单,屏幕上有三框不同颜色的球对应三种粒子:
- 质子(proton)
- 中子(neutron)
- 电子(electron)
可以直接把这些粒子拖到原子里。当加入
- 1 个质子 → 屏幕立刻显示:Hydrogen
- 再加入 1 个中子 → 似乎没有变化
- 再加入 1 个电子 → 原子变成中性
- 多加一个电子 → 原子变成带负电的离子
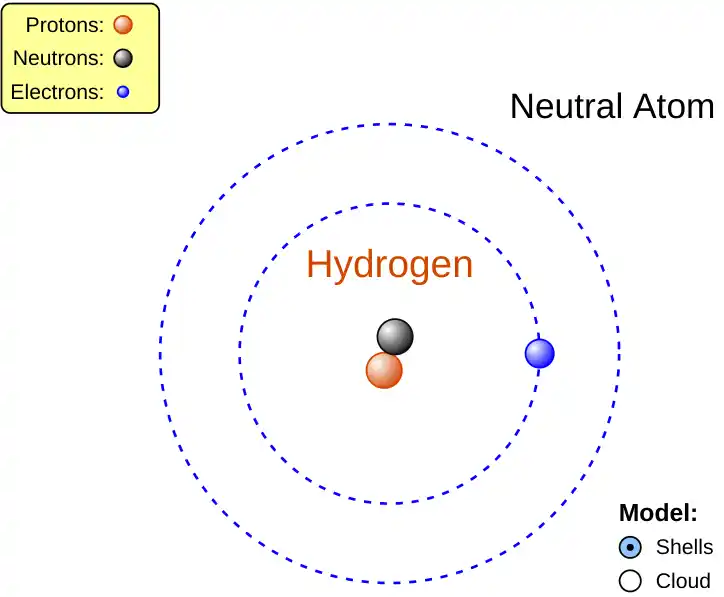
学生会马上发现:
原来“元素是什么”,只由质子的数量决定。
而电子数量决定的是“带不带电/带什么电”;中子数量决定的是“是不是同位素”。这一点,很多学生以前背了又忘,第一次在模拟里亲手操作之后,才真正理解。
我最喜欢的一幕:学生自己发现规律
传统课堂里,老师常常会直接告诉学生:
“元素编号等于质子数。”
学生记住了,但几天后又忘了。而在模拟里,我不会一开始就告诉他们答案。我会让学生自己试:
- 如果把 6 个质子变成 7 个,会发生什么?
- 如果只增加中子,会不会变成另一种元素?
- 如果删掉一个电子,为什么名字不变,但电荷变了?
很快,学生会自己总结出规律:
- 质子数改变,元素改变。
- 中子数改变,元素不变。
- 电子数改变,元素仍然不变,但会变成离子。
当规律是学生自己“发现”的时候,他们记得特别牢。
这也是为什么我一直觉得,真正有效的科学学习,不是先背定义,而是先观察、先实验、先提出问题。
科学难吗
很多学生觉得科学难,不是因为他们不够聪明,而是因为他们被要求记住结论,却从来没有真正“看见”这些结论是怎么来的。
好的教学,不只是把知识讲清楚,更重要的是让学生有机会亲手发现。
像 “Build an Atom” 这样的互动模拟,恰好能做到这一点。
延伸阅读: